„Je třeba financovat kvalitní, dostatečně robustní klinické studie s ivermektinem, aby bylo možné spolehlivě zmapovat jeho účinky při léčbě covidu-19,“ říká MUDr. Šimon Reich, který pracuje v oboru klinických studií. Podle něho nebyly dosavadní studie dobře designované a jejich výsledky vyvolávají podezření ze střetu zájmů.
Nedávno jsme informovali o tom, že americký Úřad pro kontrolu potravin a léčiv (FDA) stahuje negativní články o léčivé látce ivermektin ve spojení s onemocněním covid-19. FDA během pandemie vyzýval občany, aby jej přestali užívat k léčbě covidu, ale nyní některé články a posty na sociálních sítích po nátlaku lékařů stahuje.
V této souvislosti se široce diskutuje o cílené kampani, která měla během pandemie potlačit veškerá potenciální léčiva účinná proti novému viru SARS-CoV-2 a onemocnění covid-19, aby mohly být schváleny nové mRNA vakcíny v režimu „nouzového použití“. Dle amerických zákonů (pdf) je možné nouzové povolení udělit pouze pokud „neexistuje žádná vhodná, schválená a dostupná alternativa přípravku pro diagnostiku, prevenci nebo léčbu takového onemocnění nebo stavu“.
Stručně řečeno, pokud by bylo zjištěno, že nějaká látka účinně léčí onemocnění, nebylo by možné povolit nouzové použití vakcín.
Studie o účinnosti ivermektinu na covid-19
V České republice povolilo Ministerstvo zdravotnictví předepisovat ivermektin na léčbu covidu-19 na časové rozmezí od 12. března 2021 do 31. srpna 2021. Není nám prozatím známo, jak se vyhodnocovaly výsledky a jeho účinnost.
Podle MUDr. Šimona Reicha dospěla situace na jaře 2021 do bodu, kdy bylo dostatek informací na to, aby se začalo o využití ivermektinu během pandemie silně uvažovat.
„Tato meta-analýza randomizovaných a non-randomizovaných klinických studií za mě byla jasný signál, že pokud se do teď pochybovalo, tak nyní už je třeba ze strany států a státních institucí a organizací zafinancovat přípravu a průběh kvalitních, dostatečně robustních klinických studií s ivermektinem,“ sdělil Reich deníku The Epoch Times.
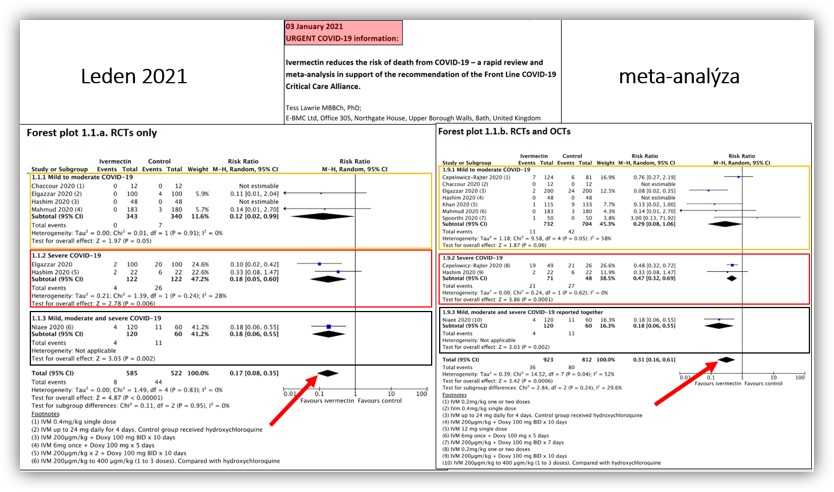
„Tuto meta-analýzu zpracovala důvěryhodná a nesmírně zkušená expertka Theresa Lawrie, která se živí tím, že podobné meta-analýzy zpracovává pro instituce jako WHO nebo Cochrane,“ dodává Reich.
Podle něho tkví problém částečně v tom, že nikdo, včetně originálního výrobce, který původně uváděl ivermektin na trh, neměl z byznysového hlediska žádnou motivaci financovat kvalitní studie, které by účinnost ivermektinu proti covid-19 mohly potvrdit.
Ivermektinu dávno vyprchala patentová ochrana a může ho proto vyrábět a prodávat každý. Jeho cena je dlouhodobě nízká a ani nová indikace tak nemůže vést k takovým ziskům jako jiné, docela nové léčivo pod čerstvou patentovou ochranou.
„Tvorba cen léčivých přípravků má svá specifická pravidla a je svým způsobem regulována,“ vysvětluje Reich. „Kromě toho se originální výrobce podílel na operaci Warp Speed, tedy na vývoji vakcín a nových preparátů proti covidu-19, v té době hojně financovaném vládou USA, což byl další důvod ivermektin přinejmenším ignorovat.“
Postupně se objevily „větší, vydatně zafinancované klinické studie“, které však podle Reicha vykazovaly problémy, které zkušený člověk z oboru může snadno vypozorovat. „Všechny tyto studie byly od začátku připravené tak, aby pokud možno vyzněly v neprospěch použití ivermektinu proti covid-19,“ míní Reich.

„Všechny velké, vydatně financované studie s ivermektinem nesou celou řadu znaků, které se tohoto týkají a v našem oboru se tomu říká designed to fail, studie od začátku připravená, navržená tak, aby neprokázala efekt studované intervence či preparátu.“
— MUDr. Šimon Reich, lékař
„Kdo v klinických studiích umí chodit a umí je do opravdu hlubokého detailu nastudovat, a správně je interpretovat, tak se všichni profesionálové, které znám, ale nevystupují v médiích, shodují na tom, že ivermektin funguje tak, že snižuje virovou nálož viru SRS CoV 2,“ říká Reich.
„Z toho vyplývá logická klinická úvaha, že například, když jsem se pohyboval mezi lidmi, kteří jsou pravděpodobně nakažení, tak to začnu brát, nebo ve chvíli, když vím, že jsem pozitivní a pravděpodobně infikovaný, tak to začnu brát. Čím později se ten preparát nasadí, tím horší má výsledky,“ popisuje účinky látky doktor Reich. „V pokročilém stavu těžkého covidu totiž odstranění původní příčiny – v tomto případě viru – už moc nepomůže bez ohledu na to, jaký preparát či preparáty pro to zvolíte.“
Jak „správně“ navrhnout studii
Studie, které se objevily, byly podle Reicha „nesmírně špatně nadesignované“ a také „nesmírně špatně až pochybně provedené“.
„Co-designoval (spolunavrhoval) jsem studie. Existují celé knihy pojednávající o tom, jak preklinickou nebo klinickou studii navrhnout a připravit tak, aby to pro váš preparát vyšlo pokud možno co nejlépe, ale stejným způsobem to lze udělat i naopak,“ vysvětluje postupy doktor Reich. „To znamená, že pokud chci, aby mi něco nevyšlo, tak jsou způsoby jak to udělat, abych zvýšil tu šanci, že mi tam efekt (preparátu) vyjde co nejmenší, přestože tam ten efekt třeba je.“
Všechny velké, vydatně financované studie s ivermektinem nesou podle Reicha „celou řadu znaků, které se tohoto týkají a v našem oboru se tomu říká designed to fail (navržená k neúspěchu)“.

„Ivermektin funguje tím způsobem, že snižuje virovou nálož viru SARS-CoV-2. Z toho logicky vyplývá, a ve studiích se to ukazuje, že nejvíce zabírá, když se užívá profylakticky (jako prevence nebo ochrana).“
— MUDr. Šimon Reich, lékař
Podle Reicha je též třeba sledovat autory studie a jejich vazby. „Jejich autoři byli lidé s obrovskými střety zájmů stejně jako i sponzoři těch studií, kteří měli vzhledem ke svým dalším investicím potenciální finanční zájem na tom, aby účinnost ivermektinu nevyšla,“ dodává Reich.
Déle nabízí přehled největších a „nejštědřeji zafinancovaných randomizovaných studií, které byly otisknuty v prestižních odborných časopisech s vysokým impakt faktorem“.
V níže uvedené tabulce popisuje v jakých aspektech byly studie špatně nastavené a odprezentované.
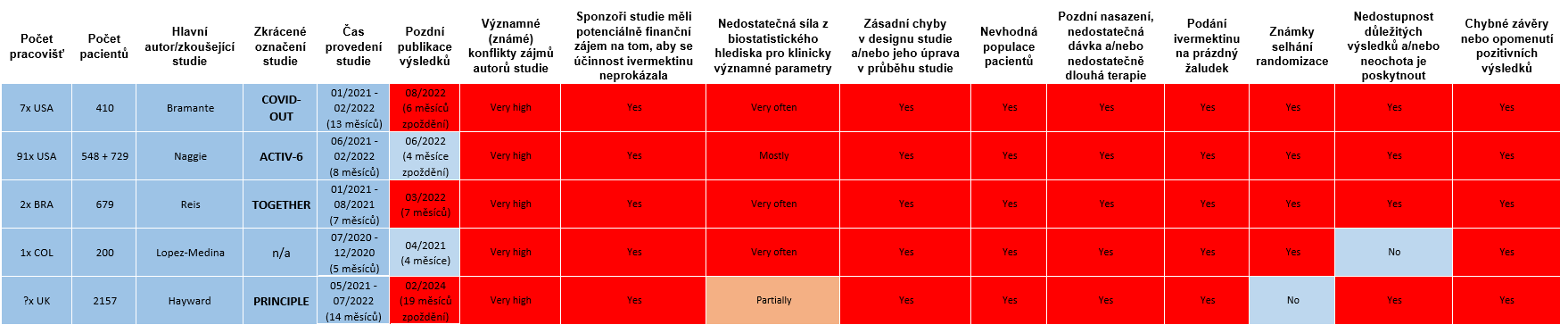
Jaké parametry by měla mít kvalitní studie
Níže uvádíme popis parametrizace kvalitní randomizované studie dle doktora Reicha a výčet studií:
- populace pacientů 50+ let se středním až vysokým rizikem těžkého průběhu covid-19 (mladí, relativně zdraví pacienti se uzdravují dobře sami bez terapie a riziko středně těžkého či těžkého průběhu je u nich apriori malé = léčbu nepotřebují),
- časné nasazení dostatečné dávky po dostatečně dlouhou dobu a dle váhy pacienta s jídlem (při podání s jídlem násobně stoupá absorpce léčiva do krve pacienta),
- vstupní změření hladiny ivermektinu v plazmě (toto dnes již roli tolik nehraje, ale tenkrát ano, protože celá řada lidí v některých regionech ivermektin užívala ještě před tím, než vstoupila do studie),
- opakované měření hladiny ivermektinu v plazmě v průběhu studie alespoň u části pacientů (kontrola, že pacienti ivermektin užívají tak, jak ho užívat mají).
Ani jedno se ani u jedné z výše uvedených studií neprovedlo, případně se proklamovalo, že se tak učinilo, ale z podrobnějšího studia dat jasně vychází, že se to nepovedlo (ať už z jakéhokoliv důvodu), konstatuje Reich.
Od začátku pandemie bylo celkem publikováno přes 160 originálních studií s ivermektinem

- 27 in silico studií (počítačové simulace)[1]
- 3 farmakokinetické studie[2]
- 21 in vitro studií (laboratorní pokusy)[3]
- 12 in vivo studií (pokusy na živých zvířatech)[4]
- 49 klinických studií randomizovaných[5]
- 56 klinických studií non-randomizovaných[6]
Klinických studií bylo tedy publikováno přibližně 103, přičemž 86 těchto prací prošlo peer-review procesem (recenzním řízením).
S negativním závěrem je pouze 22 studií (nikoliv však nutně s negativními výsledky – ve skutečnosti tyto studie nezřídka obsahují celou řadu pozitivních nálezů, které hovoří pro účinnost ivermektinu), přičemž většina z nich obsahuje spoustu zásadních chyb a rozporů, byly nezřídka připraveny a provedeny lidmi v gigantickém střetu zájmů, a je proto třeba je interpretovat velmi opatrně.
Bylo publikováno přibližně 18 přehledových článků a meta-analýz, drtivá většina z nich vyznívající pozitivně pro ivermektin.
Celkem bylo na téma ivermektin a jeho použití u onemocnění covid-19 publikováno více než 600 vědeckých článků.[7]
Zdroje:
[1] In silico studie:
1. Vottero P, Tavernini S, Santin AD, Scheim DE, Tuszynski JA, Aminpour M. Computational Prediction of the Interaction of Ivermectin with Fibrinogen. IJMS. 2023;24(14):11449. doi:10.3390/ijms241411449
2. Breitinger U, Sedky CA, Sticht H, Breitinger HG. Patch-clamp studies and cell viability assays suggest a distinct site for viroporin inhibitors on the E protein of SARS-CoV-2. Virol J. 2023;20(1):142. doi:10.1186/s12985-023-02095-y
3. Bello M. Elucidation of the inhibitory activity of ivermectin with host nuclear importin α and several SARS-CoV-2 targets. Journal of Biomolecular Structure and Dynamics. 2022;40(18):8375-8383. doi:10.1080/07391102.2021.1911857
4. Qureshi U, Mir S, Naz S, Nur-e-Alam M, Ahmed S, Ul-Haq Z. Mechanistic insights into the inhibitory activity of FDA approved ivermectin against SARS-CoV-2: old drug with new implications. Journal of Biomolecular Structure and Dynamics. 2022;40(17):8100-8111. doi:10.1080/07391102.2021.1906750
5. Ma Y, Xu X, Wu H, et al. Ivermectin contributes to attenuating the severity of acute lung injury in mice. Biomedicine & Pharmacotherapy. 2022;155:113706. doi:10.1016/j.biopha.2022.113706
6. Chellasamy SK, Watson E. Docking and molecular dynamics studies of human ezrin protein with a modelled SARS-CoV-2 endodomain and their interaction with potential invasion inhibitors. Journal of King Saud University – Science. 2022;34(7):102277. doi:10.1016/j.jksus.2022.102277
7. Alvarado YJ, Olivarez Y, Lossada C, et al. Interaction of the new inhibitor paxlovid (PF-07321332) and ivermectin with the monomer of the main protease SARS-CoV-2: A volumetric study based on molecular dynamics, elastic networks, classical thermodynamics and SPT. Computational Biology and Chemistry. 2022;99:107692. doi:10.1016/j.compbiolchem.2022.107692
8. Parvez MSA, Saha MK, Ibrahim Md, et al. Insights from a computational analysis of the SARS‐CoV‐2 Omicron variant: Host–pathogen interaction, pathogenicity, and possible drug therapeutics. Immunity Inflam & Disease. 2022;10(7):e639. doi:10.1002/iid3.639
9. Umar HI, Duru IA, Enenebeaku UE, Olehi LCN, Enyoh CE, Duru CE. Inhibitory potentials of ivermectin, nafamostat, and camostat on spike protein and some nonstructural proteins of SARS-CoV-2: Virtual screening approach. J Teknol Laboratorium. 2022;11(1):33-42. doi:10.29238/teknolabjournal.v11i1.344
10. Aminpour M, Cannariato M, Preto J, et al. In Silico Analysis of the Multi-Targeted Mode of Action of Ivermectin and Related Compounds. Computation. 2022;10(4):51. doi:10.3390/computation10040051
11. Udofia IA, Gbayo KO, Oloba-Whenu OA, Ogunbayo TB, Isanbor C. In silico studies of selected multi-drug targeting against 3CLpro and nsp12 RNA-dependent RNA-polymerase proteins of SARS-CoV-2 and SARS-CoV. Netw Model Anal Health Inform Bioinforma. 2021;10(1):22. doi:10.1007/s13721-021-00299-2
12. González-Paz L, Hurtado-León ML, Lossada C, et al. Comparative study of the interaction of ivermectin with proteins of interest associated with SARS-CoV-2: A computational and biophysical approach. Biophysical Chemistry. 2021;278:106677. doi:10.1016/j.bpc.2021.106677
13. González-Paz L, Hurtado-León ML, Lossada C, et al. Structural deformability induced in proteins of potential interest associated with COVID-19 by binding of homologues present in ivermectin: Comparative study based in elastic networks models. Journal of Molecular Liquids. 2021;340:117284. doi:10.1016/j.molliq.2021.117284
14. Rana M, Yadav P, Chowdhury P. A Computational Study of Ivermectin and Doxycycline Combination Drug Against SARS-CoV-2 Infection. Published online May 8, 2021. doi:10.21203/rs.3.rs-755838/v1
15. Schöning V, Kern C, Chaccour C, Hammann F. Highly-transmissible Variants of SARS-CoV-2 May Be More Susceptible to Drug Therapy Than Wild Type Strains. Published online April 15, 2021. doi:10.21203/rs.3.rs-379291/v1
16. Choudhury A, Das NC, Patra R, et al. Exploring the binding efficacy of ivermectin against the key proteins of SARS-CoV-2 pathogenesis: an in silico approach. Future Virology. 2021;16(4):277-291. doi:10.2217/fvl-2020-0342
17. Kern C, Schöning V, Chaccour C, Hammann F. Modeling of SARS-CoV-2 Treatment Effects for Informed Drug Repurposing. Front Pharmacol. 2021;12:625678. doi:10.3389/fphar.2021.625678
18. Prabhu PR. Virtual Screening Reveals Potential Anti-Parasitic Drugs Inhibiting the Receptor Binding Domain of SARS-CoV-2 Spike protein. 2021;10(4).
19. Francés-Monerris A, García-Iriepa C, Iriepa I, et al. Microscopic interactions between ivermectin and key human and viral proteins involved in SARS-CoV-2 infection. Phys Chem Chem Phys. 2021;23(40):22957-22971. doi:10.1039/D1CP02967C
20. Francés-Monerris A, García-Iriepa C, Iriepa I, et al. Has Ivermectin Virus-Directed Effects against SARS-CoV-2? Rationalizing the Action of a Potential Multitarget Antiviral Agent. Published online August 10, 2020.
21. Lehrer S. Ivermectin Docks to the SARS-CoV-2 Spike Receptor-binding Domain Attached to ACE2. In Vivo. 2020;34(5):4. doi:10.21873/invivo.12134
22. Swargiary A. Ivermectin as a promising RNA-dependent RNA polymerase inhibitor and a therapeutic drug against SARS-CoV2: Evidence from in silico studies. Published online September 9, 2020. doi:10.21203/rs.3.rs-73308/v1
23. Maurya DK. A Combination of Ivermectin and Doxycycline Possibly Blocks the Viral Entry and Modulate the Innate Immune Response in COVID-19 Patients. Published online July 2020:20. doi:10.26434/chemrxiv.12630539.v1
24. Suravajhala R, Parashar A, Malik B, et al. Comparative Docking Studies on Curcumin with COVID-19 Proteins. Published online July 6, 2020. doi:10.20944/preprints202005.0439.v3
25. Sen Gupta PS, Biswal S, Panda SK, Ray AK, Rana MK. Binding Mechanism and Structural Insights into the Identified Protein Target of Covid-19 with In-Vitro Effective Drug Ivermectin. Published online June 2020:20. doi:10.26434/chemrxiv.12463946.v1
26. Dayer MR. Coronavirus (2019-nCoV) Deactivation via Spike Glycoprotein Shielding by Old Drugs, Bioinformatic Study. Published online May 2020:22. doi:10.20944/preprints202005.0020.v1
27. Dasgupta J, Sen U, Bakshi A, et al. Nsp7 and Spike Glycoprotein of SARS-CoV-2 Are Envisaged as Potential Targets of Vitamin D and Ivermectin. Published online May 2020:13. doi:10.20944/preprints202005.0084.v1
[2] Farmakokinetické studie:
1. Albariqi AH, Wang Y, Chang RYK, et al. Pharmacokinetics and safety of inhaled ivermectin in mice as a potential COVID-19 treatment. International Journal of Pharmaceutics. 2022;619:121688. doi:10.1016/j.ijpharm.2022.121688
2. Arshad U, Pertinez H, Box H, et al. Prioritization of Anti‐SARS‐Cov‐2 Drug Repurposing Opportunities Based on Plasma and Target Site Concentrations Derived from their Established Human Pharmacokinetics. Clin Pharmacol Ther. 2020;108(4):15. doi:10.1002/cpt.1909
3. Errecalde J, Lifschitz A, Vecchioli G, et al. Ivermectin repurposing for COVID-19 therapy: Safety and pharmacokinetic assessment of a novel nasal spray formulation in a pig model. Published online October 2020:23. doi:10.1101/2020.10.23.352831
[3] In vitro studie:
1. Jitobaom K, Boonarkart C, Manopwisedjaroen S, et al. Synergistic anti-SARS-CoV-2 activity of repurposed anti-parasitic drug combinations. BMC Pharmacol Toxicol. 2022;23(1):41. doi:10.1186/s40360-022-00580-8
2. Boschi, Scheim, Bancod. SARS-CoV-2 Spike Protein Induces Hemagglutination: Implications for COVID-19 Morbidities and Therapeutics and for Vaccine Adverse Effects. Published online November 28, 2022.
3. De Forni D, Poddesu B, Cugia G, Chafouleas J, Lisziewicz J, Lori F. Synergistic drug combinations designed to fully suppress SARS-CoV-2 in the lung of COVID-19 patients. Bagde H, ed. PLoS ONE. 2022;17(11):e0276751. doi:10.1371/journal.pone.0276751
4. Williams T. Not All Ivermectin Is Created Equal: Comparing The Quality of 11 Different Ivermectin Sources. Published online December 6, 2022.
5. Delandre O, Gendrot M, Jardot P, et al. Antiviral Activity of Repurposing Ivermectin against a Panel of 30 Clinical SARS-CoV-2 Strains Belonging to 14 Variants. Pharmaceuticals. 2022;15(4):445. doi:10.3390/ph15040445
6. Liu J, Zhang Y, Han L, et al. Genome-wide analyses reveal the detrimental impacts of SARS-CoV-2 viral gene Orf9c on human pluripotent stem cell-derived cardiomyocytes. Stem Cell Reports. 2022;17(3):522-537. doi:10.1016/j.stemcr.2022.01.014
7. Jeffreys LN, Pennington SH, Duggan J, et al. Remdesivir–ivermectin combination displays synergistic interaction with improved in vitro activity against SARS-CoV-2. International Journal of Antimicrobial Agents. 2022;59(3):106542. doi:10.1016/j.ijantimicag.2022.106542
8. Segatori VI, Garona J, Caligiuri LG, et al. Effect of Ivermectin and Atorvastatin on Nuclear Localization of Importin Alpha and Drug Target Expression Profiling in Host Cells from Nasopharyngeal Swabs of SARS-CoV-2- Positive Patients. Viruses. 2021;13(10):2084. doi:10.3390/v13102084
9. Jitobaom K, Boonarkart C, Manopwisedjaroen S, et al. Favipiravir and Ivermectin Showed in Vitro Synergistic Antiviral Activity against SARS-CoV-2. Published online October 14, 2021. doi:10.21203/rs.3.rs-941811/v1
10. Munson. Niclosamide and ivermectin modulate caspase-1 activity and proinflammatory cytokine secretion in a monocytic cell line. Published online June 16, 2021.
11. Yesilbag K, Toker EB, Ates O. Ivermectin also inhibits the replication of bovine respiratory viruses (BRSV, BPIV-3, BoHV-1, BCoV and BVDV) in vitro. Virus Research. 2021;297:198384. doi:10.1016/j.virusres.2021.198384
12. Li N, Zhao L, Zhan X. Quantitative proteomics reveals a broad‐spectrum antiviral property of ivermectin, benefiting for COVID‐19 treatment. Journal Cellular Physiology. 2021;236(4):2959-2975. doi:10.1002/jcp.30055
13. Mody V, Ho J, Wills S, et al. Identification of 3-chymotrypsin like protease (3CLPro) inhibitors as potential anti-SARS-CoV-2 agents. Commun Biol. 2021;4(1):93. doi:10.1038/s42003-020-01577-x
14. Surnar B, Kamran MZ, Shah AS, Dhar S. Clinically Approved Antiviral Drug in an Orally Administrable Nanoparticle for COVID-19. ACS Pharmacol Transl Sci. 2020;3(6):1371-1380. doi:10.1021/acsptsci.0c00179
15. Caly L, Druce JD, Catton MG, Jans DA, Wagstaff KM. The FDA-approved drug ivermectin inhibits the replication of SARS-CoV-2 in vitro. Antiviral Res. 2020;178:4. doi:10.1016/j.antiviral.2020.104787
16. Zheng J, Lu C, Ding Y, et al. Red blood cell-hitchhiking mediated pulmonary delivery of ivermectin: Effects of nanoparticle properties. International Journal of Pharmaceutics. 2022;619:121719. doi:10.1016/j.ijpharm.2022.121719
17. Saha T, Sinha S, Harfoot R, Quiñones-Mateu ME, Das SC. Manipulation of Spray-Drying Conditions to Develop an Inhalable Ivermectin Dry Powder. Pharmaceutics. 2022;14(7):1432. doi:10.3390/pharmaceutics14071432
18. Mountain Valley MD. In Vitro and mouse study with human ACE2 cells, using solubilized ivermectin with Ivectosol™. Published online May 2021.
19. Liu J, Wu S, Zhang Y, et al. SARS-CoV-2 viral genes Nsp6, Nsp8, and M compromise cellular ATP levels to impair survival and function of human pluripotent stem cell-derived cardiomyocytes. Stem Cell Res Ther. 2023;14(1):249. doi:10.1186/s13287-023-03485-3
20. García-Aguilar A, Campi-Caballero R, Visoso-Carvajal G, et al. In Vitro Analysis of SARS-CoV-2 Spike Protein and Ivermectin Interaction. IJMS. 2023;24(22):16392. doi:10.3390/ijms242216392
21. Fauquet J, Carette J, Duez P, Zhang J, Nachtergael A. Microfluidic Diffusion Sizing Applied to the Study of Natural Products and Extracts That Modulate the SARS-CoV-2 Spike RBD/ACE2 Interaction. Molecules. 2023;28(24):8072. doi:10.3390/molecules28248072
[4] In vivo studie:
1. Uematsu T, Takano T, Matsui H, Kobayashi N, Ōmura S, Hanaki H. Prophylactic administration of ivermectin attenuates SARS-CoV-2 induced disease in a Syrian Hamster Model. J Antibiot. 2023;76(8):481-488. doi:10.1038/s41429-023-00623-0
2. Abd-Elmawla MA, Ghaiad HR, Gad ES, Ahmed KA, Abdelmonem M. Suppression of NLRP3 inflammasome by ivermectin ameliorates bleomycin-induced pulmonary fibrosis. J Zhejiang Univ Sci B. 2023;24(8):723-733. doi:10.1631/jzus.B2200385
3. Ma Y, Xu X, Wu H, et al. Ivermectin contributes to attenuating the severity of acute lung injury in mice. Biomedicine & Pharmacotherapy. 2022;155:113706. doi:10.1016/j.biopha.2022.113706
4. Albariqi AH, Wang Y, Chang RYK, et al. Pharmacokinetics and safety of inhaled ivermectin in mice as a potential COVID-19 treatment. International Journal of Pharmaceutics. 2022;619:121688. doi:10.1016/j.ijpharm.2022.121688
5. Zheng J, Lu C, Ding Y, et al. Red blood cell-hitchhiking mediated pulmonary delivery of ivermectin: Effects of nanoparticle properties. International Journal of Pharmaceutics. 2022;619:121719. doi:10.1016/j.ijpharm.2022.121719
6. M. Mansour S, N. Shamma R, A. Ahmed K, et al. Safety of inhaled ivermectin as a repurposed direct drug for treatment of COVID-19: A preclinical tolerance study. International Immunopharmacology. 2021;99:108004. doi:10.1016/j.intimp.2021.108004
7. Mountain Valley MD. Mountain Valley MD Receives Successful Results From BSL-4 COVID-19 Clearance Trial on Three Variants Tested With IvectosolTM. Published online May 18, 2021.
8. Chaccour C, Abizanda G, Irigoyen-Barrio Á, et al. Nebulized ivermectin for COVID-19 and other respiratory diseases, a proof of concept, dose-ranging study in rats. Sci Rep. 2020;10(1):11. doi:10.1038/s41598-020-74084-y
9. de Melo GD, Lazarini F, Larrous F, et al. Anti-COVID-19 efficacy of ivermectin in the golden hamster. Published online November 2020:20. doi:10.1101/2020.11.21.392639
10. Arévalo A, Pagotto R, Pórfido J, et al. Ivermectin reduces coronavirus infection in vivo: a mouse experimental model. Published online November 2020:32. doi:10.1101/2020.11.02.363242
11. Errecalde J, Lifschitz A, Vecchioli G, et al. Ivermectin repurposing for COVID-19 therapy: Safety and pharmacokinetic assessment of a novel nasal spray formulation in a pig model. Published online October 2020:23. doi:10.1101/2020.10.23.352831
12. Mountain Valley MD. In Vitro and mouse study with human ACE2 cells, using solubilized ivermectin with IvectosolTM. Published online May 2021.
[5] Randomizované studie:
1. Wada. Efficacy and safety of single-dose ivermectin in mild-to-moderate COVID-19: the double-blind, randomized, placebo-controlled CORVETTE-01 trial. Frontiers in Medicine. Published online May 22, 2023.
2. Desort-Henin. The SAIVE Trial, Post-Exposure use of ivermectin in Covid-19 prevention: Efficacy and Safety Results. Published online January 5, 2023.
3. Schilling. Pharmacometrics of high dose ivermectin in early COVID‐19: an open label, randomized, controlled adaptive platform trial (PLATCOV). Published online February 21, 2023.
4. Sarojvisut. An Open Label Randomized Controlled Trial of Ivermectin Plus Favipiravir-Based Standard of Care versus Favipiravir-Based Standard of Care for Treatment of Moderate COVID-19 in Thailand. Infection & Chemotherapy. Published online December 12, 2022.
5. de la Rocha. Ivermectin compared with placebo in the clinical course in Mexican patients with asymptomatic and mild COVID-19: a randomized clinical trial. Published online August 12, 2022.
6. Ochoa-Jaramillo. Clinical efficacy and safety of ivermectin (400 μg/kg, single dose) in patients with severe COVID-19: a randomized clinical trial. Published online October 21, 2022.
7. Aref. Possible Role of Ivermectin Mucoadhesive Nanosuspension Nasal Spray in Recovery of Post-COVID-19 Anosmia. Published online September 19, 2022.
8. Bramante. Randomized Trial of Metformin, Ivermectin, and Fluvoxamine for Covid-19. New England Journal of Medicine. Published online August 18, 2022.
9. Mirahmadizadeh. Efficacy of single-dose and double-dose ivermectin early treatment in preventing progression to hospitalization in mild COVID-19: A multi-arm, parallel-group randomized, double-blind, placebo-controlled trial. Published online June 23, 2022.
10. Rezai. Non-effectiveness of Ivermectin on Inpatients and Outpatients With COVID-19; Results of Two Randomized, Double-Blinded, Placebo-Controlled Clinical Trials. Frontiers in Medicine. Published online June 16, 2022.
11. Naggie. Ivermectin for Treatment of Mild-to-Moderate COVID-19 in the Outpatient Setting: A Decentralized, Placebo-controlled, Randomized, Platform Clinical Trial. JAMA. Published online December 6, 2022.
12. George. Single Dose of Ivermectin is not Useful in Patients with Hematological Disorders and COVID-19 Illness: A Phase II B Open Labelled Randomized Controlled Trial. Published online May 27, 2022.
13. Reis G, Silva EASM, Silva DCM, et al. Effect of Early Treatment with Ivermectin among Patients with Covid-19. N Engl J Med. 2022;386(18):1721-1731. doi:10.1056/NEJMoa2115869
14. Beltran Gonzalez JL, González Gámez M, Mendoza Enciso EA, et al. Efficacy and Safety of Ivermectin and Hydroxychloroquine in Patients with Severe COVID-19: A Randomized Controlled Trial. Infectious Disease Reports. 2022;14(2):160-168. doi:10.3390/idr14020020
15. Lim SCL, Hor CP, Tay KH, et al. Efficacy of Ivermectin Treatment on Disease Progression Among Adults With Mild to Moderate COVID-19 and Comorbidities: The I-TECH Randomized Clinical Trial. JAMA Intern Med. Published online February 18, 2022. doi:10.1001/jamainternmed.2022.0189
16. Manomaipiboon A, Pholtawornkulchai K, Pupipatpab S, et al. Efficacy and safety of ivermectin in the treatment of mild-to-moderate COVID-19 infection: A randomized, double blind, placebo, controlled trial. Published online February 2022. doi:10.21203/rs.3.rs-1290999/v1
17. Buonfrate D. High-dose ivermectin for early treatment of COVID-19 (COVER study): a randomised, double-blind, multicentre, phase II, dose-finding, proof-of-concept clinical trial. International Journal of Antimicrobial Agents. Published online January 1, 2022:9.
18. Abbas KU, Muhammad S, Ding SF. The Effect of Ivermectin on Reducing Viral Symptoms in Patients with Mild COVID-19. Indian Journal of Pharmaceutical Sciences. 2022;(1):5.
19. Vallejos J, Zoni R, Bangher M, et al. Ivermectin to prevent hospitalizations in patients with COVID-19 (IVERCOR-COVID19) a randomized, double-blind, placebo-controlled trial. BMC Infect Dis. 2021;21(1):635. doi:10.1186/s12879-021-06348-5
20. Okumuş N, Demirtürk N, Çetinkaya RA, et al. Evaluation of the effectiveness and safety of adding ivermectin to treatment in severe COVID-19 patients. BMC Infect Dis. 2021;21(1):411. doi:10.1186/s12879-021-06104-9
21. Krolewiecki A. Antiviral effect of high-dose ivermectin in adults with COVID-19: A proof-of-concept randomized trial. Published online June 2021:8.
22. Chachla MP. A randomized trial – intensive treatment based in ivermectin and iota-carrageenan as pre-exposure prophylaxis for covid- 19 in healthcare agents. Published online June 2021:29.
23. Aref ZF, Bazeed SEES, Hassan MH, et al. Clinical, Biochemical and Molecular Evaluations of Ivermectin Mucoadhesive Nanosuspension Nasal Spray in Reducing Upper Respiratory Symptoms of Mild COVID-19. IJN. 2021;Volume 16:4063-4072. doi:10.2147/IJN.S313093
24. Shahbaznejad L, Davoudi A, Eslami G, et al. Effects of Ivermectin in Patients With COVID-19: A Multicenter, Double-Blind, Randomized, Controlled Clinical Trial. Clinical Therapeutics. Published online May 2021:13. doi:10.1016/j.clinthera.2021.04.007
25. Seet RCS, Quek AML, Ooi DSQ, et al. Positive impact of oral hydroxychloroquine and povidone-iodine throat spray for COVID-19 prophylaxis: An open-label randomized trial. International Journal of Infectious Diseases. 2021;106:314-322. doi:10.1016/j.ijid.2021.04.035
26. Mahmud R, Rahman MdM, Alam I, et al. Ivermectin in combination with doxycycline for treating COVID-19 symptoms: a randomized trial. J Int Med Res. 2021;49(5):030006052110135. doi:10.1177/03000605211013550
27. Chahla RE, Ruiz LM, Mena T, et al. Cluster Randomised Trials – Ivermectin Repurposing For COVID-19 Treatment Of Outpatients With Mild Disease In Primary Health Care Centers. Published online May 2021. doi:10.21203/rs.3.rs-495945/v1
28. Faisal R, Shah SFA, Hussain M. Potential use of azithromycin alone and in combination with ivermectin in fighting against the symptoms of COVID-19. TPMJ. 2021;28(05):5. doi:10.29309/TPMJ/2021.28.05.5867
29. Bukhari KH, Asghar A, Perveen N, et al. Efficacy of Ivermectin in COVID-19 Patients with Mild to Moderate Disease. Published online May 2021. doi:10.1101/2021.02.02.21250840
30. Biber A, Mandelboim M, Harmelin G, et al. Favorable outcome on viral load and culture viability using Ivermectin in early treatment of non-hospitalized patients with mild COVID-19, A double-blind, randomized placebo-controlled trial. Published online May 2021:23. doi:10.1101/2021.05.31.21258081
31. Abd-Elsalam S. Clinical study evaluating the efficacy of ivermectin in COVID‐19. Journal of Medical Virology. Published online May 2021.
32. López-Medina E, López P, Hurtado IC, et al. Effect of Ivermectin on Time to Resolution of Symptoms Among Adults With Mild COVID-19: A Randomized Clinical Trial. JAMA. Published online April 4, 2021:10. doi:10.1001/jama.2021.3071
33. Huvemek. Kovid-19 – Huvemek® Phase 2 clinical trial.pdf. Published online March 25, 2021.
34. Pott-Junior H, Paoliello MMB, Miguel A de QC, et al. Use of ivermectin in the treatment of Covid-19: A pilot trial. Toxicology Reports. 2021;8:505-510. doi:10.1016/j.toxrep.2021.03.003
35. Chowdhury abu taiub mohammed mohiuddin, Shahbaz, Karim, Islam, Dan, He. A Comparative Study on Ivermectin-Doxycycline and Hydroxychloroquine-Azithromycin Therapy on COVID-19 Patients. EJMO. Published online February 25, 2021:8. doi:10.14744/ejmo.2021.16263
36. Mohan A, Tiwari P, Suri T, et al. Ivermectin in mild and moderate COVID-19 (RIVET-COV): a randomized, placebo-controlled trial. Published online February 2, 2021:21. doi:10.21203/rs.3.rs-191648/v1
37. Shoumann WM, Hegazy AA, Nafae RM, et al. Use of Ivermectin as a Potential Chemoprophylaxis for COVID-19 in Egypt: A Randomized Clinical Trial. Journal of Clinical and Diagnostic Research. 2021;15:6.
38. Babalola, Bode, Ajayi, et al. Ivermectin shows clinical benefits in mild to moderate COVID19: A randomised controlled double-blind, dose-response study in Lagos. QJM: An International Journal of Medicine. Published online January 18, 2021:34.
39. Ravikirti, Roy R, Pattadar C, et al. Ivermectin as a potential treatment for mild to moderate COVID-19 – A double blind randomized placebo-controlled trial. Published online September 1, 2021:14. doi:10.1101/2021.01.05.21249310
40. Chaccour C, Casellas A, Blanco-Di Matteo A, et al. The effect of early treatment with ivermectin on viral load, symptoms and humoral response in patients with non-severe COVID-19: A pilot, double-blind, placebo-controlled, randomized clinical trial. EClinicalMedicine. 2021;32:100720. doi:10.1016/j.eclinm.2020.100720
41. Ahmed S, Karim MM, Ross AG, et al. A five-day course of ivermectin for the treatment of COVID-19 may reduce the duration of illness. International Journal of Infectious Diseases. 2020;103:2. doi:10.1016/j.ijid.2020.11.191
42. Hashim HA, Maulood MF, Rasheed AM, Fatak DF, Kabah KK, Abdulamir AS. Controlled randomized clinical trial on using Ivermectin with Doxycycline for treating COVID-19 patients in Baghdad, Iraq. Published online October 27, 2020:14. doi:10.1101/2020.10.26.20219345
43. Podder CS, Chowdhury N, Sina MI, Haque WMU. Outcome of ivermectin treated mild to moderate COVID-19 cases: a single-centre, open-label, randomised controlled study. Published online March 9, 2020:8.
44. Chachar AZK, Khan KA, Asif M, Khaqan A, Basri R. Effectiveness of Ivermectin in SARS-CoV-2/COVID-19 Patients. 2020;9:5.
45. Kishoria N. Ivermectin as adjuvant to hydroxycholoroquine in patients resistant to standard treatment for sars-cov-2: results of an open-label randomized clinical study. PIJR. Published online August 23, 2020:4.
46. Siripongboonsitti T, et. al. A randomized trial to assess the acceleration of viral clearance by the combination Favipiravir/Ivermectin/Niclosamide in mild-to-moderate COVID-19 adult patients (FINCOV). Journal of Infection and Public Health. 2024;17(5):897-905. doi:10.1016/j.jiph.2024.03.030
47. ACTIV-6 Group. ACTIV-6: Operationalizing a decentralized, outpatient randomized platform trial to evaluate efficacy of repurposed medicines for COVID-19. J Clin Trans Sci. 2023;7(1):e221. doi:10.1017/cts.2023.644
48. Hayward G, Yu LM, Little P, et al. Ivermectin for COVID-19 in adults in the community (PRINCIPLE): An open, randomised, controlled, adaptive platform trial of short- and longer-term outcomes. Journal of Infection. 2024;88(4):106130. doi:10.1016/j.jinf.2024.106130
49. El-Tanani M, Ahmed KAA, Shakya AK, Ammari WG, Al-Shudifat AE. Phase II, Double-Blinded, Randomized, Placebo-Controlled Clinical Trial Investigating the Efficacy of Mebendazole in the Management of Symptomatic COVID-19 Patients. Pharmaceuticals. 2023;16(6):799. doi:10.3390/ph16060799
[6] Non-randomizované studie:
1. Osati E, Shayo GA, Nagu T, et al. Clinical manifestations and mortality among hospitalized COVID-19 patients in Tanzania, 2021-2022. Published online July 16, 2023. doi:10.1101/2023.07.13.23292643
2. Llenas-García J, Del Pozo A, Talaya A, et al. Ivermectin Effect on In-Hospital Mortality and Need for Respiratory Support in COVID-19 Pneumonia: Propensity Score-Matched Retrospective Study. Viruses. 2023;15(5):1138. doi:10.3390/v15051138
3. Munir MZ, Khan AH, Khan TM. Clinical Disease Characteristics and Treatment Trajectories Associated with Mortality among COVID-19 Patients in Punjab, Pakistan. Healthcare. 2023;11(8):1192. doi:10.3390/healthcare11081192
4. Ozer M, Goksu SY, Conception R, et al. Effectiveness and safety of Ivermectin in COVID‐19 patients: A prospective study at a safety‐net hospital. Journal of Medical Virology. 2022;94(4):1473-1480. doi:10.1002/jmv.27469
5. Qadeer R, Kashif SM, Kumar D, Mehmmood M, Lal J, . F. Ivermectin A Potential Treatment In Covid-19, Related to Critical Illness. PJMHS. 2022;16(8):24-26. doi:10.53350/pjmhs2216824
6. Ravikirti, Ranjan A, Porel R, et al. Association between Ivermectin treatment and mortality in Covid-19: A hospital-based case-control study. Published online June 4, 2022. doi:10.21203/rs.3.rs-1522422/v1
7. Shimizu K, Hirata H, Kabata D, et al. Ivermectin administration is associated with lower gastrointestinal complications and greater ventilator-free days in ventilated patients with COVID-19: A propensity score analysis. Journal of Infection and Chemotherapy. 2022;28(4):548-553. doi:10.1016/j.jiac.2021.12.024
8. Ascencio-Montiel IDJ, Tomás-López JC, Álvarez-Medina V, et al. A Multimodal Strategy to Reduce the Risk of Hospitalization/death in Ambulatory Patients with COVID-19. Archives of Medical Research. 2022;53(3):323-328. doi:10.1016/j.arcmed.2022.01.002
9. Soto A, Quiñones-Laveriano DM, Azañero J, et al. Mortality and associated risk factors in patients hospitalized due to COVID-19 in a Peruvian reference hospital. Serra R, ed. PLoS ONE. 2022;17(3):e0264789. doi:10.1371/journal.pone.0264789
10. Mustafa ZU, Kow CS, Salman M, et al. Pattern of medication utilization in hospitalized patients with COVID-19 in three District Headquarters Hospitals in the Punjab province of Pakistan. Exploratory Research in Clinical and Social Pharmacy. 2022;5:100101. doi:10.1016/j.rcsop.2021.100101
11. Hazan S, Dave S, Gunaratne AW, et al. Effectiveness of ivermectin-based multidrug therapy in severely hypoxic, ambulatory COVID-19 patients. Future Microbiology. 2022;17(5):339-350. doi:10.2217/fmb-2022-0014
12. Efimenko I, Nackeeran S, Jabori S, Zamora JAG, Danker S, Singh D. Treatment with Ivermectin Is Associated with Decreased Mortality in COVID-19 Patients: Analysis of a National Federated Database. International Journal of Infectious Diseases. 2022;116:S40. doi:10.1016/j.ijid.2021.12.096
13. Zubair SM, Chaudhry MW, Zubairi ABS, et al. The effect of ivermectin on non-severe and severe COVID-19 disease and gender-based difference of its effectiveness. Monaldi Arch Chest Dis. Published online January 18, 2022. doi:10.4081/monaldi.2022.2062
14. Kerr L, Cadegiani FA, Baldi F, et al. Ivermectin Prophylaxis Used for COVID-19: A Citywide, Prospective, Observational Study of 223,128 Subjects Using Propensity Score Matching. Cureus. Published online January 15, 2022. doi:10.7759/cureus.21272
15. Baguma S, Okot C, Onira NA, et al. Characteristics of the COVID-19 patients treated at Gulu Regional Referral Hospital, Northern Uganda: A cross-sectional study. Published online December 28, 2021. doi:10.21203/rs.3.rs-1193578/v1
16. Jamir L, Tripathi M, Shankar S, Kakkar R, Ayyanar R, Aravindakshan R. Determinants of Outcome Among Critically Ill Police Personnel With COVID-19: A Retrospective Observational Study From Andhra Pradesh, India. Cureus. Published online December 13, 2021. doi:10.7759/cureus.20394
17. Samajdar SS, Mukherjee S, Mondal T, et al. Ivermectin and Hydroxychloroquine for Chemo-Prophylaxis of COVID-19: A Questionnaire Survey of Perception and Prescribing Practice of Physicians vis-à-vis Outcomes. Published online November 2021.
18. Rezk N, Elsayed Sileem A, Gad D, Khalil A. miRNA-223-3p, miRNA- 2909 and Cytokines Expression in COVID-19 Patients Treated with Ivermectin. Zagazig University Medical Journal. 2021;0(0):0-0. doi:10.21608/zumj.2021.92746.2329
19. Mukarram MS. Ivermectin Use Associated with Reduced Duration of Covid-19 Febrile Illness in a Community Setting. IJCMCR. 2021;13(4). doi:10.46998/IJCMCR.2021.13.000320
20. Cadegiani FA, Goren A, Wambier CG, McCoy J. Early COVID-19 therapy with azithromycin plus nitazoxanide, ivermectin or hydroxychloroquine in outpatient settings significantly improved COVID-19 outcomes compared to known outcomes in untreated patients. New Microbes and New Infections. 2021;43:100915. doi:10.1016/j.nmni.2021.100915
21. Morgenstern J, Redondo JN, Olavarria A, et al. Ivermectin as a SARS-CoV-2 Pre-Exposure Prophylaxis Method in Healthcare Workers: A Propensity Score-Matched Retrospective Cohort Study. Cureus. Published online August 26, 2021. doi:10.7759/cureus.17455
22. Elavarasi A, Raju Sagiraju HK, Garg RK, et al. Clinical features, demography and predictors of outcomes of SARS-CoV-2 infection in a tertiary care hospital in India-A cohort study. Published online December 8, 2021. doi:10.1101/2021.08.10.21261855
23. Behera P, Patro BK, Padhy BM, et al. Prophylactic Role of Ivermectin in Severe Acute Respiratory Syndrome Coronavirus 2 Infection Among Healthcare Workers. Cureus. Published online August 5, 2021. doi:10.7759/cureus.16897
24. Faisal R, Shah SFA, Hussain M. Potential use of azithromycin alone and in combination with ivermectin in fighting against the symptoms of COVID-19. TPMJ. 2021;28(05):5. doi:10.29309/TPMJ/2021.28.05.5867
25. Ahsan T, Rani B, Siddiqui R, et al. Clinical Variants, Characteristics, and Outcomes Among COVID-19 Patients: A Case Series Analysis at a Tertiary Care Hospital in Karachi, Pakistan. Cureus. Published online April 29, 2021. doi:10.7759/cureus.14761
26. Pierre L, Christine F. Ivermectin and COVID-19 in Care Home: Case Report. J Infect Dis Epidemiol. 2021;7(4). doi:10.23937/2474-3658/1510202
27. Mourya S, Thakur AS, Hada DS, Kulshreshtha VS. Comparative Analytical Study of Two Different Drug Regimens in Treatment of Covid 19 Positive Patients in Index Medical College Hospital and Research Center, Indore, India. Published online April 2021:3.
28. Lima-Morales R, Méndez-Hernández P, Flores YN, et al. Effectiveness of a multidrug therapy consisting of Ivermectin, Azithromycin, Montelukast, and Acetylsalicylic acid to prevent hospitalization and death among ambulatory COVID-19 cases in Tlaxcala, Mexico. International Journal of Infectious Diseases. 2021;105:598-605. doi:10.1016/j.ijid.2021.02.014
29. Tanioka H, Tanioka S, Kaga K. Why COVID-19 is not so spread in Africa: How does Ivermectin affect it? Published online March 26, 2021. doi:10.1101/2021.03.26.21254377
30. Hector C, Roberto H. Safety and Efficacy of the Combined Use of Ivermectin, Dexamethasone, Enoxaparin and Aspirina against COVID-19 the I.D.E.A. Protocol. Published online September 3, 2021.
31. Behera P, Patro BK, Singh AK, et al. Role of ivermectin in the prevention of SARS-CoV-2 infection among healthcare workers in India: A matched case-control study. Adrish M, ed. PLoS ONE. 2021;16(2):e0247163. doi:10.1371/journal.pone.0247163
32. Elalfy H, Besheer T, El‐Mesery A, et al. Effect of a combination of Nitazoxanide, Ribavirin and Ivermectin plus zinc supplement (MANS.NRIZ study) on the clearance of mild COVID‐19. J Med Virol. Published online February 2021:25. doi:10.1002/jmv.26880
33. Rajter JC, Sherman MS, Fatteh N, Vogel F, Sacks J, Rajter JJ. Use of Ivermectin Is Associated With Lower Mortality in Hospitalized Patients With Coronavirus Disease 2019. Chest. 2021;159(1):85-92. doi:10.1016/j.chest.2020.10.009
34. Hellwig MD. A COVID-19 prophylaxis? Lower incidence associated with prophylactic administration of ivermectin. International Journal of Antimicrobial Agents. 2021;57(1):4. doi:10.1016/j.ijantimicag.2020.106248
35. Ferreira RM, Beranger RW, Sampaio PPN, Mansur Filho J, Lima RAC. Outcomes associated with Hydroxychloroquine and Ivermectin in hospitalized patients with COVID-19: a single-center experience. Rev Assoc Med Bras. 2021;67(10):1466-1471. doi:10.1590/1806-9282.20210661
36. Mondal S, Singha A, Das D, et al. Prevalence of COVID-19 Infection and Identification of Risk Factors among Asymptomatic Healthcare Workers : A Serosurvey Involving Multiple Hospitals in West Bengal. Journal of the Indian Medical Association. 2021;119(5).
37. Alam MT, Murshed R, Gomes PF, et al. Ivermectin as Pre-exposure Prophylaxis for COVID-19 among Healthcare Providers in a Selected Tertiary Hospital in Dhaka – An Observational Study. EJMED. 2020;2(6). doi:10.24018/ejmed.2020.2.6.599
38. Khan MdSI, Khan MdSI, Debnath CR, et al. Ivermectin Treatment May Improve the Prognosis of Patients With COVID-19. Archivos de Bronconeumología (English Edition). 2020;56(12):2. doi:10.1016/j.arbr.2020.08.011
39. Gómez-Hernández MT, Novoa NM, Antúnez P, Jiménez MF. Twice Lucky: Elderly Patient Surviving Both COVID-19 and Serendipitous Lung Carcinoma. Archivos de Bronconeumología. 2020;56(12):826-828. doi:10.1016/j.arbres.2020.07.009
40. Bernigaud C, Guillemot D, Ahmed-Belkacem A, et al. Bénéfice de l’ivermectine : de la gale à la COVID-19, un exemple de sérendipité. Annales de Dermatologie et de Vénéréologie. 2020;147(12):A194. doi:10.1016/j.annder.2020.09.231
41. Afsar N, Ghauri MI, Abbas M, Mukarram MS, Peracha MY, Ishaq K. Ivermectin Use Associated with Reduced Duration of COVID-19 Febrile Illness in a Community Setting. SSRN Journal. Published online December 2020:29. doi:10.2139/ssrn.3734478
42. Budhiraja S, Soni A, Jha V, et al. Clinical Profile of First 1000 COVID-19 Cases Admitted at Tertiary Care Hospitals and the Correlates of their Mortality: An Indian Experience. Published online November 18, 2020. doi:10.1101/2020.11.16.20232223
43. Héctor C, Roberto H, Psaltis A, Veronica C. Study of the Efficacy and Safety of Topical Ivermectin + Iota-Carrageenan in the Prophylaxis against COVID-19 in Health Personnel. J biomed res clin investig. 2020;2(1). doi:10.31546/2633-8653.1007
44. Carvallo H, Hirsch R, Alkis P, Contreras V. Study of the Efficacy and Safety of Topical Ivermectin + Iota-Carrageenan in the Prophylaxis against COVID-19 in Health Personnel. J biomed res clin investig. 2020;2(1):6. doi:10.31546/2633-8653.1007
45. Camprubí D, Almuedo-Riera A, Martí-Soler H, et al. Lack of efficacy of standard doses of ivermectin in severe COVID-19 patients. Dorlo TPC, ed. PLoS ONE. 2020;15(11):e0242184. doi:10.1371/journal.pone.0242184
46. Szente Fonseca SN, De Queiroz Sousa A, Wolkoff AG, et al. Risk of hospitalization for Covid-19 outpatients treated with various drug regimens in Brazil: Comparative analysis. Travel Medicine and Infectious Disease. 2020;38:101906. doi:10.1016/j.tmaid.2020.101906
47. Spoorthi V. Utility of Ivermectin and Doxycycline combination for the treatment of SARS-CoV-2. International Archives of Integrated Medicine. Published online October 2020:6.
48. Soto-Becerra P, Culquichicón C, Hurtado-Roca Y, Araujo-Castillo RV. Real-world effectiveness of hydroxychloroquine, azithromycin, and ivermectin among hospitalized COVID-19 patients: results of a target trial emulation using observational data from a nationwide healthcare system in Peru. Published online October 2020:25.
49. Chamie J. Real-World Evidence: The Case of Peru. Published online September 2020:26.
50. Carvallo H, Hirsch R, Farinella María E. Safety and Efficacy of the combined use of ivermectin, dexamethasone, enoxaparin and aspirin against COVID 19. Published online September 2020:10. doi:10.1101/2020.09.10.20191619
51. Espitia-Hernandez G, Munguia L, Diaz-Chiguer D, Lopez-Elizalde R. Effects of Ivermectin-azithromycin-cholecalciferol combined therapy on COVID-19 infected patients: A proof of concept study. Biomed Res. 2020;31(5):5.
52. Gorial FI, Mashhadani S, Sayaly HM, et al. Effectiveness of Ivermectin as add-on Therapy in COVID-19 Management (Pilot Trial). Published online August 7, 2020. doi:10.1101/2020.07.07.20145979
53. Saavedra C, Cerna Y, Figueredo T, Masías C. Post-acute or prolonged covid-19: treatment with ivermectin for patients with persistent, or post-acute symptoms. Published online July 2020:1.
54. Ramos WM, Pérez MAGM, Acosta AC, et al. Intervención de la Ivermectina Pre-Hospitalariapara la Modificación de la Evolución del Covid19. Estudio realizado en Perú. Published online June 16, 2020.
55. Alam MT, Murshed R, Bhiuyan E, Saber S, Alam RF, Robin RC. A Case Series of 100 COVID-19 Positive Patients Treated with Combination of Ivermectin and Doxycycline. J Bangladesh Coll Phys. Published online December 6, 2020:5. doi:10.3329/jbcps.v38i0.47512
56. Procter B, Ross C, Pickard Vanessa, Smith E, Hanson C, McCullough PA. Clinical outcomes after early ambulatory multidrug therapy for high-risk SARS-CoV-2 (COVID-19) infection. Reviews in Cardiovascular Medicine. 2020;21(4):611. doi:10.31083/j.rcm.2020.04.260
[7] Přehledové články a meta-analýzy:
1. Ragó Z, Tóth B, Szalenko-Tőkés Á, et al. Results of a systematic review and meta-analysis of early studies on ivermectin in SARS-CoV-2 infection. GeroScience. Published online March 7, 2023. doi:10.1007/s11357-023-00756-y
2. CovidAnalysis. Ivermectin for COVID-19 Real-Time Meta-Analysis of 248 Studies; 2024.
3. Hariyanto TI, Halim DA, Rosalind J, Gunawan C, Kurniawan A. Ivermectin and outcomes from Covid‐19 pneumonia: A systematic review and meta‐analysis of randomized clinical trial studies. Reviews in Medical Virology. 2022;32(2). doi:10.1002/rmv.2265
4. Chakraborty C, Sharma AR, Bhattacharya M, Agoramoorthy G, Lee SS. The Drug Repurposing for COVID-19 Clinical Trials Provide Very Effective Therapeutic Combinations: Lessons Learned From Major Clinical Studies. Front Pharmacol. 2021;12:704205. doi:10.3389/fphar.2021.704205
5. Santin AD, Scheim DE, McCullough PA, Yagisawa M, Borody TJ. Ivermectin: a multifaceted drug of Nobel prize-honoured distinction with indicated efficacy against a new global scourge, COVID-19. New Microbes and New Infections. 2021;43:6. doi:10.1016/j.nmni.2021.100924
6. Bryant A, Lawrie TA, Dowswell T, et al. Ivermectin for Prevention and Treatment of COVID-19 Infection: A Systematic Review, Meta-analysis, and Trial Sequential Analysis to Inform Clinical Guidelines. Am J Ther. 2021;28(4):27. doi:10.1097/MJT.0000000000001402
7. Nardelli P, Zangrillo A, Sanchini Gabriele. Crying wolf in time of Corona: the strange case of ivermectin and hydroxychloroquine. Is the fear of failure withholding potential life-saving treatment from clinical use? SV. Published online August 5, 2021. doi:10.22514/sv.2021.043
8. Descotes J. MEDICAL SAFETY OF IVERMECTIN. Published online March 3, 2021.
9. IVMMETA.COM. Ivermectin is effective for COVID-19: real-time meta analysis of 42 studies. Published online February 2021:30.
10. Lawrie TA. Ivermectin reduces the risk of death from COVID-19 – a rapid review and meta-analysis in support of the recommendation of the Front Line COVID-19 Critical Care Alliance. Published online January 2021:21.
11. Kory P, Meduri GU, Iglesias J, et al. Review of the Emerging Evidence Demonstrating the Efficacy of Ivermectin in the Prophylaxis and Treatment of COVID-19. Published online January 2021:30.
12. Hill A. Preliminary meta analysis of randomized trials of ivermectin to treat SARS-CoV-2. Published online January 2021:36.
13. FLCCC. One-Page-Summary-of-the-Clinical-Trials-Evidence-for-Ivermectin-in-COVID-19. Published online January 2021:1.
14. Kalfas S, Visvanathan K, Chan K, Drago J. The Therapeutic Potential Of Ivermectin For COVID-19: A Systematic Review Of Mechanism And Evidence. Published online December 2020:17.
15. Heidary F. Ivermectin: a systematic review from antiviral effects to COVID-19 complementary regimen. J Antibiot. 2020;73(9):10. doi:10.1038/s41429-020-0336-z
16. McCullough PA, Alexander, Armstrong. Multifaceted highly targeted sequential multidrug treatment of early ambulatory high-risk SARS-CoV-2 infection (COVID-19). Reviews in Cardiovascular Medicine. 2020;21(4):517. doi:10.31083/j.rcm.2020.04.264
[7] Celkový počet vědeckých článků na téma ivermektin a covid19: